製品特性および投与イメージ
- 日本初の注腸フォーム製剤です。
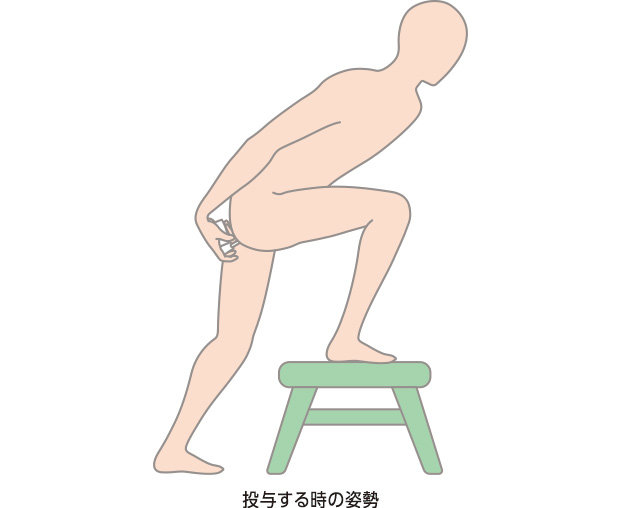
- 泡が直腸~S状結腸までひろがり、とどまることで、漏れにくく、立ったままで投与できます。
- 国内第Ⅲ相試験において、主要評価項目である粘膜治癒率【6週】は32.8%でプラセボに対する優越性が検証されました(尤度比検定 p<0.0001)。
- 有効成分ブデソニドのバイオアベイラビリティは約16%と推察され、体内に吸収後は肝臓で代謝を受けます。
-
承認時までの国内の臨床試験では175例中95例(54.3%)に臨床検査値異常を含む副作用が認められました。主な副作用は血中コルチゾール減少72例(41.1%)、血中コルチコトロピン減少62例(35.4%)でした。
添付文書の副作用及び臨床成績の安全性の結果を参照ください。
製剤写真

投与イメージ