■反復投与10)
日本人のアントラサイクリン系抗悪性腫瘍剤の血管外漏出患者(成人)2例に、デクスラゾキサンを1日1回90分かけて3日間連日静脈内投与したときの薬物動態を検討しました。
反復投与時の薬物動態パラメータ
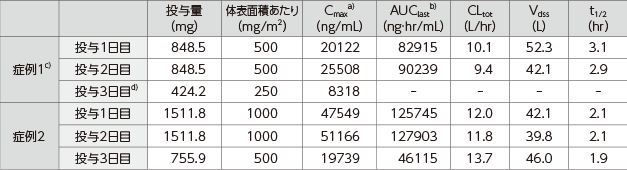
Cmax:最高血漿中濃度、 AUC:血中濃度- 時間曲線下面積、 CLtot :全身クリアランス、 Vdss:定常状態分布容積、 t1/2:消失半減期
a) 投与終了直後
b) 投与1~3日目の各投与における投与開始時から血漿中薬物濃度定量可能最終時点(投与1日目及び2日目:次投与直前、投与3日目:投与終了4時間後)までのAUC
c) 腎機能低下が認められたため、実施計画書の規定に従い、デクスラゾキサンの投与量を通常の半量とした。また、本症例においては血漿中薬物動態パラメータの算出は本薬投与1日目及び2日目(本薬投与3日目の投与直前まで)を対象とした。
d) 投与終了直後の1ポイントのみの測定であった。
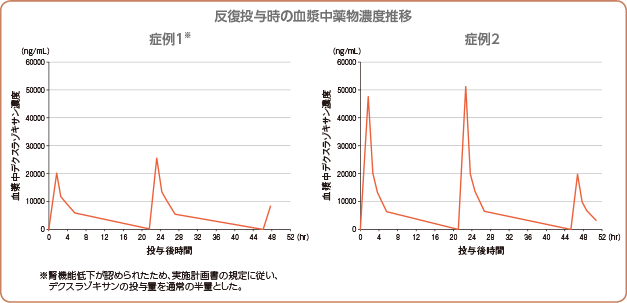
承認時評価資料:国内第Ⅰ/Ⅱ相臨床試験(KDX1101)
投与1日目及び2日目は1000mg/m2を、3日目は500mg/m2を1日1回90分かけて3日間連日静脈内投与した。
9. 特定の背景を有する患者に関する注意(一部抜粋)
- 9.2 腎機能障害患者
- 血液毒性の発現に注意して観察すること。デクスラゾキサンは大部分が腎排泄されることが知られており、腎機能障害のある患者では、本剤の排泄率が低下し、全身への曝露時間が延長する可能性があることから、副作用が強くあらわれるおそれがある。[16.6.1参照]
■参考:反復投与(外国人データ)11)
アントラサイクリン系抗悪性腫瘍剤の血管外漏出患者(外国人)6例を対象として、投与1日目及び2日目はデクスラゾキサン1000mg/m2を、3日目は500mg/m2を1日1回1~2時間かけて、3日間連日静脈内投与したときの薬物動態を検討しました。
ノンコンパートメントモデルで評価した結果、投与1日目及び2日目における24時間血中濃度-時間曲線下面積はほぼ同様であり、反復投与による蓄積は認められませんでした。
反復投与時の薬物動態パラメータ
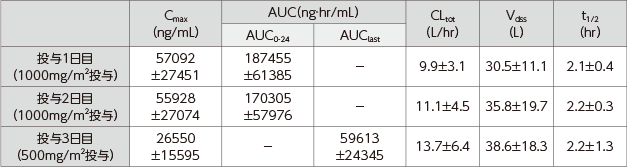
Mean ± SD
Cmax:最高血漿中濃度、 AUC:血中濃度- 時間曲線下面積、 CLtot :全身クリアランス、 Vdss:定常状態分布容積、t1/2:消失半減期
承認時評価資料:海外市販後臨床試験(TT04)
■特別な患者集団(腎機能低下症例、 外国人データ)10)
腎機能の程度が異なる24例※の男女を対象に、150mg/m2のデクスラゾキサンを一定速度で15分間静脈内投与したときの薬物動態を検討した結果、全身クリアランスは腎機能低下者で低下し、中等度及び重度の腎機能低下者の無限時間までの血中濃度-時間曲線下面積は腎機能正常者と比べて2倍高値を示しました。
用量調節のシミュレーションにおいて、クレアチニンクリアランスが40mL/min未満の患者では、投与量を50%にすることで、腎機能正常者と同等の曝露(無限時間までの血中濃度-時間曲線下面積)が達成されることが示唆されました。
※ 正常(80mL/min<クレアチニンクリアランス):6例
軽度低下(50mL/min<クレアチニンクリアランス≦80mL/min):5例
中等度低下(30mL/min<クレアチニンクリアランス≦50mL/min):6例
重度低下(クレアチニンクリアランス≦30mL/min):7例
Brier ME. et al.:J Clin Pharmacol. 51, 731, 2011
- 6. 用法及び用量
- 通常、成人には、デクスラゾキサンとして、1日1回、投与1日目及び2日目は1000mg/m2(体表面積)、3日目は500mg/m2を1~2時間かけて3日間連続で静脈内投与する。なお、血管外漏出後6時間以内に可能な限り速やかに投与を開始し、投与2日目及び3日目は投与1日目と同時刻に投与を開始する。また、用量は、投与1日目及び2日目は各2000mg、3日目は1000mgを上限とする。
中等度及び高度の腎機能障害のある患者(クレアチニンクリアランス:40mL/min未満)では投与量を通常の半量とする。
9. 特定の背景を有する患者に関する注意(一部抜粋)
- 9.2 腎機能障害患者
- 血液毒性の発現に注意して観察すること。デクスラゾキサンは大部分が腎排泄されることが知られており、腎機能障害のある患者では、本剤の排泄率が低下し、全身への曝露時間が延長する可能性があることから、副作用が強くあらわれるおそれがある。[16.6.1参照]
デクスラゾキサンは体内に分布し、タンパク結合率は2%未満でした。がん性胸水の患者における胸水中の濃度は、血漿中の10~100%と幅がありました。
承認時評価資料:分布
■代謝物(外国人データ14)
デクスラゾキサンは生体内で2種類の中間代謝物に代謝されはじめ、中間代謝物Bの濃度はデクスラゾキサン濃度の8~29%、中間代謝物Cの濃度はデクスラゾキサン濃度の3〜5%でした。その後、これらの代謝物もADR-925に代謝され(15分で最高濃度に到達後、半減期2.5時間と0.6時間で消失)、血清中から半減期24時間で消失しました。
Schroeder PE, et al.:Cancer Chemother Pharmacol. 52, 167, 2003
■代謝経路(in vitro)15)
デクスラゾキサンは加水分解を受け、2種類の中間代謝物を経てADR-925に代謝されると考えられます。
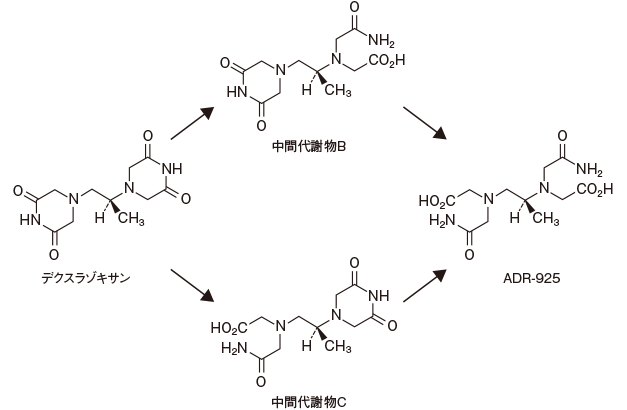
中間代謝物B:(2S)-N-(Carbamoylmethyl)[1-(3,5-dioxopiperazin-1-yl)propan-2-yl]aminoacetic acid
中間代謝物C:(2S)-N-(Carbamoylmethyl)[2-(3,5-dioxopiperazin-1-yl)propyl]aminoacetic acid
ADR-925:(2S)-N,N'-(Propane-1,2-diyl)bis[N-(carbamoylmethyl)aminoacetic acid]
承認時評価資料:代謝経路
成人では投与量の34~48%が尿中へ排泄され、小児では同60%が尿中へ排泄されました。胆汁中への排泄は1例において検討され、24時間で1%未満であることが示されました。
承認時評価資料:排泄